On n’a jamais autant parlé de thérapie génique qu’en ce moment, que ce soit dans les journaux spécialisés ou autour de la machine à café des services. À force de voir des communiqués triomphants sur de soi-disant “guérisons révolutionnaires”, il n’est pas rare de ressentir un mélange d’espoir, de curiosité… et d’un brin de scepticisme. Derrière les grandes annonces, que faut-il vraiment retenir de ces traitements ? Où en est la pratique sur le terrain, en quoi consiste-t-elle concrètement, et qu’est-ce qu’un professionnel ou un patient peut raisonnablement attendre pour aujourd’hui et demain ? Je vous propose une plongée sans jargon stérile, mais avec la rigueur de quelqu’un qui, comme vous, veut démêler le vrai du fantasme.
Comprendre la thérapie génique : petites causes, grands effets
De quoi parle-t-on ? Maladies génétiques et innovations ciblées
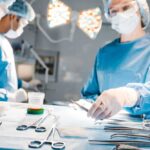
À l’hôpital, combien de fois ai-je croisé des familles désemparées face à une maladie rare, cette fameuse “erreur dans le code génétique” dont on parle comme d’une fatalité ? La thérapie génique, elle, s’attaque directement au problème à la racine : le gène. L’idée — brillante mais loin d’être “magique” — est simple sur le papier : corriger, remplacer ou inactiver un gène défectueux pour restaurer une fonction ou prévenir l’apparition des symptômes.
Là où la médecine classique agit surtout sur les conséquences (l’inflammation, la douleur, etc.), la thérapie génique aborde les causes sur un plan moléculaire, souvent avec des techniques ultra ciblées comme CRISPR-Cas9 ou les vecteurs viraux (ces fameux “virus modifiés” utilisés comme cheval de Troie, oui, j’ai vu l’œil inquiet de quelques collègues !).
Quand une patiente — appelons-la Camille — m’a confié qu’un laboratoire testait sur son fils une “injection qui pourrait réparer son ADN”, j’ai vu dans ses yeux l’ampleur de l’espoir misé dans ce mot : thérapie génique. Mais entre l’annonce et la réalité, il y a tout un monde de contraintes éthiques, de protocoles et de patience…
Applications actuelles : du rêve à la réalité sur le terrain
Plusieurs domaines bénéficient déjà, dans une certaine mesure, des avancées de la thérapie génique. Voyons ce qu’il en est, sans langue de bois :
- Maladies génétiques rares : hémophilie, amyotrophie spinale, certaines formes de cécité (comme l’amaurose congénitale de Leber)… Dans ces cas très ciblés, des thérapies comme le Zolgensma® ou le Luxturna® ont officiellement changé la donne (et le visage de certains “cas insolubles”).
- Cancers : Les CAR-T cells (chimiothérapie personnalisée basée sur les lymphocytes modifiés génétiquement) ont ouvert une brèche, particulièrement dans les leucémies et lymphomes agressifs réfractaires.
- Maladies neurologiques : Les premiers signalements d’amélioration motrice substantielle chez des patients atteints de maladie de Parkinson traités par vecteur viral ont attiré l’attention… même si on reste loin de la généralisation.
Je me rappelle cette discussion un peu musclée avec un chef de service : “Michel, ton machin, c’est un coup de pub, non ?” — Même scepticisme chez d’anciens collègues. Pourtant, les chiffres sont là : selon l’AFM-Téléthon, plus de 2 000 essais cliniques sont en cours sur la planète, et les traitements autorisés quittent leur statut de “miracle isolé” pour s’installer peu à peu dans l’arsenal thérapeutique réel.
| Indication | Traitement génique | Coût estimé (par traitement) | État d’avancement |
|---|---|---|---|
| Amaurose congénitale de Leber | Luxturna® | 700 000 € | Commercialisé |
| Atrophie musculaire spinale (SMA) | Zolgensma® | 1,9 million € | Commercialisé |
| Leucémie aiguë lymphoblastique pédiatrique | CAR-T cells | 350 000 à 410 000 € | Commercialisé (Accès contrôlé) |
| Drepanocytose (drépanocytose) | CRISPR/Vertex® | En attente (prix inconnu) | Phase III d’essai |
Du laboratoire à la vraie vie : entre résultats et limites
Les résultats les plus frappants : guérisons, mais à quel prix ?
Difficile de ne pas être impressionné par certaines histoires : des enfants condamnés par la SMA à une paralysie rapide, qui retrouvent motricité et sourire après une seule injection ; des adultes aveugles regagnant quelques dixièmes sur l’échelle de la vision. Ces cas existent, ils sont spectaculaires, et encore plus bouleversants quand on regarde les vidéos avant/après.
Mais la médaille a son revers. La plupart de ces traitements coûtent plus cher qu’une maison familiale, aussi bien au niveau financier que logistique. Et tous ne réussissent pas : il reste des échecs, des effets secondaires parfois graves (réaction immunitaire sévère, hépatotoxicité, etc.), et un suivi à long terme qui, parfois, laisse planer le doute. On ne guérit pas toujours, mais on ouvre une porte thérapeutique.
Dans mon parcours, j’ai pu accompagner un jeune patient hémophile sous thérapie génique expérimentale. Trois mois d’hôpital, douze médecins autour de la table, et une famille suspendue au bilan sanguin. D’un côté, une nette amélioration ; de l’autre, une vigilance de tous les instants sur la persistance de l’efficacité et l’absence de complications imprévues. Même victoire, on reste humble.
Entre fantasme et prudence : quels enjeux pour le patient et le système ?
On entend parfois des promesses du type : « Dans 5 ans, toutes les maladies génétiques seront guérissables ! »… C’est oublier la complexité humaine. L’individualisation du traitement, la réponse immunitaire, les variants génétiques, l’accès aux essais cliniques (souvent réservé aux “bons cas” avec critères stricts)… Autant de barrières réelles à l’universalisation, du moins à court terme.
Techniquement, le délai entre la découverte d’un gène et le traitement curatif s’étend rarement sous la décennie. Même la médecine personnalisée bute sur le coût : combien de systèmes de santé peuvent aujourd’hui prendre en charge une injection à 2 millions d’euros, même une seule fois ?
Côté patient, il y a l’attente, parfois cruelle. Et côté soignant, la lourdeur du parcours de soins : INCa, HCL, AMM… Trois sigles, des dizaines de réunions pluridisciplinaires. En France, deux patients sur trois éligibles à un traitement génique ne peuvent encore accéder effectivement à la molécule. La grande bascule n’a pas encore eu lieu, mais l’évolution est tangible.
Les perspectives : demain s’invente aujourd’hui
CRISPR et la révolution de l’édition génétique
Si vous deviez ne retenir qu’un mot pour votre prochaine partie de Trivial Pursuit, choisissez CRISPR. Cet outil, qui a valu le Prix Nobel de Chimie à ses inventrices, permet une modification très fine et ciblée du génome, presque comme si l’on utilisait une gomme à effacer sur une page (bon, ça reste une image un peu naïve, mais elle marche bien lors des ateliers avec les étudiants !).
Des premiers essais sur la drépanocytose ou la bêta-thalassémie donnent des résultats prometteurs. On commence à voir émerger des projets de thérapie génique “à la carte”, où la médecine devient un mix entre ingénieur et artisan : chaque patient, un génome, un logiciel (presque) unique.
La question n’est plus de savoir “si” la thérapie génique s’imposera, mais “comment” l’intégrer dans un système éthique, équitable, et sécurisé. Les débats (parfois animés !) sur les limites, la transgénèse, la modification d’embryons — et bien sûr la fameuse protection des données de santé — animent les conférences depuis des années. Heureusement, la vigilance collective (professionnels de santé, bioéthiciens, patients) reste un garde-fou salutaire.
Vers une accessibilité plus large
Un point central dans mon quotidien de formateur, c’est la question de l’accès. La majorité des malades concernés ne vivent ni à Paris, ni à Boston, et n’ont pas la bonne mutation parfaitement cartographiée sur leur dossier : comment leur ouvrir la porte à ces innovations ?
Des initiatives, comme le compassionate use et l’ouverture de centres de référence, émergent. Les industriels négocient — non sans tensions — des prix à la baisse, et la recherche française se positionne (parfois à la surprise générale !) comme leader en certains domaines.
Il reste tout de même une réalité : on ne pourra pas transposer, du jour au lendemain, ces avancées à la totalité de notre patientèle. Mais pour une tranche, même réduite, l’espoir n’a jamais été aussi tangible.
Défis et freins à lever pour la décennie à venir
Questions de sécurité, éthique et suivi à long terme
Si je devais résumer ce que je ressens devant chaque nouvelle “victoire” médiatique de la thérapie génique, ce serait : enthousiasme… tempéré d’une grande prudence.
- Sécurité à long terme : Peut-on garantir l’absence d’effet délétère vingt ou trente ans après l’administration ? À ce jour, le recul manque.
- Réponse immunitaire : Certains patients développent une immunisation contre le vecteur viral, rendant le traitement inopérant ou dangereux en cas de nouvelle injection.
- Éthique : Où placer la limite ? Modifier un gène pour sauver une vie, d’accord. Mais l’utiliser pour booster la mémoire ou la force physique, on entre sur un tout autre terrain…
- Suivi médico-social : Impossible de se contenter d’une “injection miracle”. Cela implique de revoir le suivi au long cours, la coordination entre équipes spécialisées et le partage des données (en toute sécurité !).
L’expérience du terrain me confirme qu’en France, comme ailleurs, le système avance souvent plus lentement que la technologie. Mais je préfère cela à la précipitation — le diable se cache dans les détails, et sur une chaîne ADN, le moindre détail compte…
Enjeux économiques et organisationnels
Parlons franchement : le financement est LE mur d’escalade actuel. Un traitement à plusieurs centaines de milliers d’euros, c’est non seulement un casse-tête pour l’Assurance Maladie, mais aussi un défi pour le choix des bénéficiaires. Qui, quoi, comment prioriser ?
Des modèles exportés permettent d’imaginer des forfaits sur 5 ou 10 ans, des remboursements conditionnés à l’efficacité réelle (pay-for-performance), ou des synergies avec l’assurance privée. Rien n’est simple, mais la réflexion avance, et chacun de nous peut prendre part, même modestement, à ce chantier d’équité.
Un chemin plein de promesses : prendre le tournant en équipe
Si je me retourne sur les deux dernières décennies, l’écart entre les rêves de labo et la réalité hospitalière se resserre. On avance, parfois à petits pas, parfois par bonds prodigieux. La thérapie génique, ce n’est ni la panacée, ni un simple effet de mode. C’est une nouvelle dimension qui s’ouvre à la médecine : celle où chaque patient peut espérer que son histoire soit réécrite dès la source.
J’encourage chacun, professionnel ou non, à s’informer, à échanger, à questionner : Où en est l’accès à ces traitements dans mon établissement ? Comment informer au mieux mes patients ? Quels freins puis-je lever à mon échelle ? La santé connectée, c’est aussi ça : un dialogue constant entre l’humain, la technique, et l’éthique.
Et vous, quelle place accordez-vous à la thérapeutique de demain dans votre parcours ? En parler, c’est déjà faire avancer la réflexion commune. Les portes de l’innovation s’ouvrent plus grand si on les pousse ensemble !
FAQ sur la thérapie génique
Qu’est-ce que la thérapie génique ?
C’est une approche thérapeutique qui consiste à introduire, modifier ou supprimer un gène dans l’organisme, avec l’objectif de corriger une anomalie à l’origine d’une maladie. On utilise pour cela des vecteurs (souvent des virus désactivés) ou, plus récemment, des outils d’édition comme CRISPR.
Quels types de maladies peuvent aujourd’hui être traités par la thérapie génique ?
Les principales applications concernent pour l’instant certaines maladies génétiques rares (comme la SMA, l’amaurose de Leber), des cancers (via les cellules CAR-T) et des troubles neurologiques ciblés. Mais le champ des indications s’élargit rapidement avec la recherche.
Quels sont les résultats observés chez les patients ?
Chez certains patients, les bénéfices sont spectaculaires : amélioration marquée, voire disparition des symptômes pour des maladies autrefois “incurables”. Mais il existe aussi des cas d’échec ou des effets secondaires exigeant un suivi renforcé.
Quels sont les principaux défis ou risques associés ?
Outre le coût élevé, le suivi à long terme est indispensable : risque de réaction immunitaire, complications imprévues sur le plan génétique… et bien sûr, d’importantes questions éthiques à propos des modifications transmissibles à la descendance.
Quel avenir pour la thérapie génique en France et en Europe ?
L’accès devrait progressivement s’améliorer, à mesure que les prix baissent et que de nouvelles indications reçoivent une autorisation. La vigilance restera de mise pour garantir la sécurité et l’équité d’accès à ces avancées majeures de la médecine moderne.